Epidemiologia
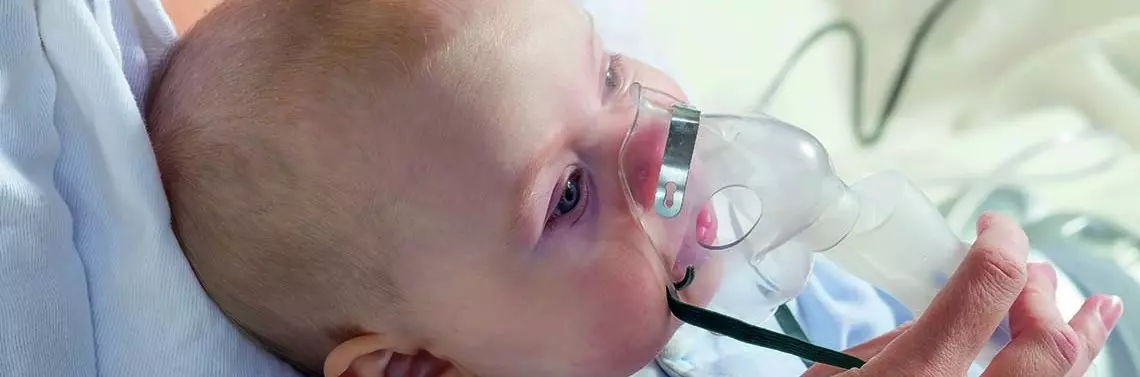
Populacja ryzyka ciężkiego zachorowania obejmuje noworodki urodzone przed 35. tygodniem trwania ciąży, dzieci z dysplazją oskrzelowo-płucną (BPD) i dzieci z hemodynamicznie istotną wadą serca [1, 2]. Do zagrażającego życiu pogorszenia wydolności oddechowej po zakażeniu wirusem RS dochodzić może także we wrodzonych chorobach takich jak mukowiscidoza, rdzeniowy zanik mięśni (SMA) i zespół ciężkiego niedoboru odporności.
Obraz kliniczny zakażeń RSV
Zakażenie wirusem RS (syncytium nabłonka oddechowego) wywołuje zmiany zapalne o różnym nasileniu: u starszych dzieci i dorosłych – banalne infekcje kataralne (nieżyt nosa, złe samopoczucie, z gorączką lub bez niej, osłuchowo – szmer pęcherzykowy, furczenia udzielone), ale u noworodków i niemowląt (podczas pierwszego zakażenia) najczęściej dochodzi do zapalenia płuc lub zapalenia oskrzelików [4, 5]. Wynika to z niedojrzałej budowy dróg oddechowych, wąskich oskrzeli łatwo ulegających dodatkowej obturacji w przebiegu zmian zapalnych i niedojrzałości mechanizmów odpornościowych z brakiem przeciwciał uzyskanych od matki przed urodzeniem. Dochodzi do zwężenia oskrzelików, co utrudnia przepływ powietrza. Wydzielany w nadmiarze śluz zatyka oskrzeliki (zwłaszcza końcowe), dlatego pewna ilość powietrza dostaje się do pęcherzyków płucnych, ale nie może się z nich wydostać. Ten efekt zastawkowy jest powodem nadmiernego rozdęcia płuc.
Objawy chorobowe są bardzo zróżnicowane: nieefektywny kaszel, tachypnoe, duszność wydechowa ze świstem (w nomenklaturze angielskiej nazywanym wheezingiem), wzmożony wysi...
Pozostałe 90% treści dostępne jest tylko dla Prenumeratorów
- 6 wydań czasopisma "Forum Pediatrii Praktycznej"
- Nielimitowany dostęp do całego archiwum czasopisma
- Dodatkowe artykuły niepublikowane w formie papierowej
- ...i wiele więcej!

Dołącz do grona pediatrów - praktyków, którzy stale pogłębiają swoją wiedzę
Co dwa miesiące otrzymuj algorytmy diagnostyczne i aktualne wytyczne leczenia dzieci, tworzone przez doświadczonych lekarzy – praktyków.