Etiologia
Istotą schorzenia w klasycznej postaci są zaburzenia wchłaniania spowodowane przewlekłym autoimmunizacyjnym stanem zapalnym w jelicie cienkim. U osób predysponowanych genetycznie, w wyniku kontaktu z glutenem oraz pokrewnymi prolaminami, dochodzi do powstawania przeciwciał przeciwko transglutaminazie tkankowej (tTG) i endomysium mięśni gładkich (EMA) oraz odpowiedzi komórkowej. Te mechanizmy prowadzą do uszkodzenia i zaniku kosmków jelitowych, rozrostu krypt, a to z kolei do biegunki oraz zaburzeń wchłaniania.
Przebieg kliniczny
Istnieje wiele różnych klasyfikacji celiakii, najczęściej wyróżnia się postaci: klasyczną, atypową, niemą, latentną oraz potencjalną.
Dawniej dominowała postać klasyczna nietolerancji glutenu z objawami z przewodu pokarmowego, tzn. biegunką tłuszczową, bólami brzucha, postępującą utratą masy ciała, dużym brzuchem, cienkimi kończynami, krzywicą i niedokrwistością z niedoboru żelaza.
Obecnie dużo częściej obserwuje się postaci atypowe, dlatego w nazewnictwie można spotkać podział na postaci z objawami pochodzącymi z przewodu pokarmowego oraz spoza niego (tab. 1).
Tab. 1. Objawy celiakii z i spoza przewodu pokarmowego
| Objawy z przewodu pokarmowego | Objawy spoza przewodu pokarmowego |
| Biegunka Zaparcie Ból brzucha Zaburzenia łaknienia Utrata masy ciała |
Zmiany skórne (choroba Duhringa) Osteoporoza, osteopenia Anemia z niedoboru żelaza Zaburzenia miesiączkowania, niepłodność Niskorosłość Skaza krwotoczna Podwyższone enzymy wątrobowe, trzustkowe Polineuropatia Zaburzenia mineralizacji szkliwa Zaburzenia nastroju, intelektualne Depresja |
Jako celiakię niemą rozumie się obecność przeciwciał celiakalnych, antygenów HLA typowych dla celiakii i zaniku kosmków w badaniu histopatologicznym skrawków z dwunastnicy, ale bez towarzyszących objawów. Celiakia potencjalna to taka, w której nie doszło jeszcze do zaniku kosmków. Postać latentna rozpoznawana jest u osób, którym na pewnym etapie życia towarzyszyła objawowa enteropatia, a obecnie nie ma objawów.
Choroba trzewna może objawiać się jako wyżej wspomniana postać klasyczna, trzeba jej jednak też poszukiwać u osób z izolowanymi objawami, takimi jak np. trudno lecząca się niedokrwistość z niedoboru żelaza, niedobory masy ciała i/lub wzrostu, zaburzenia miesiączkowania, niepłodność, hipertransaminazemia, depresja, stany lękowe.
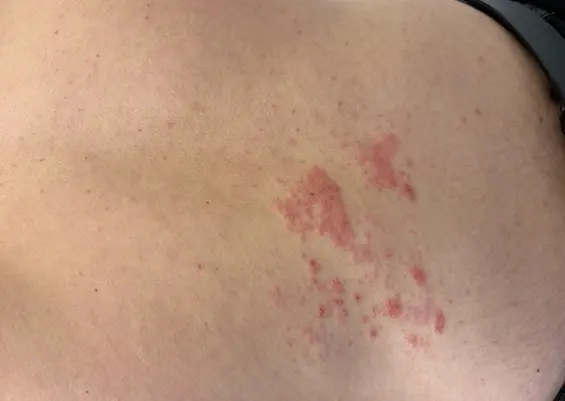
Szczególną postacią jest choroba Duhringa, czyli opryszczkowate zapalenie skóry. Jest to tzw. skórna postać celiakii, spowodowana odkładaniem się złogów IgAEMA w skórze. Zmiany skórne o charakterze pęcherzyków, grudek czy rumienia pojawiają się najczęściej na pośladkach, łokciach, plecach i okolicy kości krzyżowej – towarzyszy im świąd. Charakterystyczną dla niego cechą jest zaostrzanie się pod wpływem jodu. Należy ją podejrzewać zwłaszcza u osób z obciążonym wywiadem rodzinnym i objawami złego wchłaniania.
Najgroźniejszym późnym powikłaniem źle leczonej lub nieleczonej celiakii jest chłoniak jelita cienkiego.
Rozpoznawanie
W diagnostyce celiakii wykorzystuje się obecnie metody serologiczne, endoskopowe (histopatologiczne) oraz genetyczne.
W diagnostyce serologicznej określa się miano przeciwciał przeciw transglutaminazie tkankowej (tTG), przeciwendomyzjalnych (EMA) oraz przeciw deamidowanej gliadynie (DGP). Mają one wysoką czułość i swoistość.
Najgroźniejszym późnym powikłaniem źle leczonej lub nieleczonej celiakii jest chłoniak jelita cienkiego.
W diagnostyce serologicznej należy pamiętać, że celiakii często towarzyszy niedobór IgA i dlatego powinno się oznaczyć całkowite stężenie IgA, a przy stwierdzeniu niedoboru IgA lub jego braku oznaczać przeciwciała również w klasie IgG. Odeszło się już od oznaczania innych przeciwciał, np. przeciwgliadynowych, z uwagi na ich niską czułość.
Do rozpoznania choroby trzewnej nie wystarczy sama obecność swoistych przeciwciał. U części osób, pomimo utrzymywania się ich obecności we krwi, nie dochodzi do rozwoju enteropatii. U osób podejrzanych o celiakię należy dodatkowo wykonać gastroduodenoskopię i pobrać z opuszki dwunastnicy oraz jej części zstępującej wycinki do badania histopatologicznego. Skrócenie kosmków, obecność IEL (limfocytów śródnabłonkowych) oraz rozrost krypt (typ 2 i 3 według Marsha) przemawiają za celiakią.
Od pewnego czasu wiadomo, że u ponad 95% osób chorujących na enteropatię glutenową występuje charakterystyczny układ genów zgodności tkankowej, czyli HLA-DQ2 i/lub HLA-DQ8. Brak tych antygenów praktycznie wyklucza rozpoznanie celiakii.
Według najnowszych wytycznych ESPGHAN (styczeń 2012) u dzieci, u których tTG przekraczają 10 razy normę, obecne są EMA oraz wynik badania genetycznego jest dodatni, można odejść od wykonywania biopsji dwunastnicy. We wszystkich pozostałych przypadkach jej wykonanie to warunek konieczny do postawienia rozpoznania.
Obecnie nie jest wymagana prowokacja glutenem w celu potwierdzenia choroby. Wykonuje się ją w wybranych, wątpliwych przypadkach, zawsze jednak powinna być poprzedzona badaniem genetycznym. Nie ma konkretnych zaleceń, ile powinna trwać i po jakim czasie jej trwania trzeba wykonywać badania diagnostyczne. Uznaje się, że w okresie prowokacji pacjent powinien spożywać normalną ilość glutenu, tj. ok. 15 g na dobę (0,5 g/kg m.c./dobę).
Nigdy, poza sytuacją ewidentnej, ciężkiej alergicznej reakcji natychmiastowej na gluten, nie należy zlecać diety bezglutenowej przed wykluczeniem celiakii, gdyż wtedy do potwierdzenia lub wykluczenia celiakii potrzeba niekiedy wielu lat oraz konieczne jest przeprowadzenie testu prowokacji, obciążającego chorego, narażającego go na niepotrzebne badania (w tym endoskopia) i niepotrzebnie indukującego zmiany chorobowe w jelicie.
Warto pamiętać, że celiakia może towarzyszyć innym chorobom autoimmunizacyjnym (chorobie Hashimoto, nieswoistemu zapaleniu jelit, reumatoidalnemu zapaleniu stawów), zespołom genetycznym (Downa, Turnera), niedoborowi IgA oraz występować w rodzinach predysponowanych genetycznie. U tych osób należy zbadać obecność DQ2/DQ8 lub okresowo kontrolować obecność swoistych przeciwciał. Bardziej szczegółowe wskazania do wykonywania badań przesiewowych w kierunku celiakii przedstawia tab. 2.
Tab. 2. Wskazania do diagnostyki przesiewowej w kierunku celiakii
| Wskazania do diagnostyki w kierunku celiakii | |
| Wywiad | Charakterystyczne objawy |
| Wywiad rodzinny | Krewni I i II stopnia |
| Choroby autoimmunologiczne |
|
| Choroby genetyczne |
|
| Inne | Niedobór/brak IgA |
Leczenie
Celiakia jest chorobą (choć nie zawsze jawną) trwającą całe życie, a jedynym jej skutecznym leczeniem jest ścisłe przestrzeganie diety bezglutenowej. Gluten jest to białko występujące w pszenicy, życie i jęczmieniu. Ze względu na możliwość zanieczyszczenia owsa innymi zbożami, czy to w czasie uprawy, czy też na etapie obróbki przemysłowej, uznaje się, że nie jest on bezpieczny dla osób chorych na celiakię.
Ważne jest dokładne sprawdzanie składu spożywanych produktów; częstym, nieświadomie popełnianym błędem dietetycznym jest przyjmowanie glutenu z tzw. ukrytych źródeł. Może się on znajdować w różnego rodzaju wędlinach, słodyczach, przetworach mlecznych, przyprawach zawierających glutaminian sodu.
Czas od wprowadzenia diety bezglutenowej do zaniku przeciwciał celiakalnych we krwi zależy od ich miana wyjściowego, przyjmuje się jednak, że powinno się to stać w ciągu roku.
W początkowym okresie leczenia, zwłaszcza u osób z nasiloną biegunką, konieczne może być wprowadzenie diety bezlaktozowej – z uwagi na wtórną do skrócenia kosmków nietolerancję laktozy. Ponadto część chorych wymaga suplementacji wapnia i/lub żelaza.
Produkty dozwolone i zakazane w diecie chorych na celiakię zestawiono w tab. 3.
Tab. 3. Produkty dozwolone i zabronione w diecie bezglutenowej
| Produkty dozwolone | Produkty zabronione |
| Mleko płynne i w proszku Sery, twarogi, śmietana Sery żółte Wszystkie mięsa Podroby – wątroba, płuca, nerki Ryby Jaja Wszystkie owoce i warzywa Orzechy Ryż, kukurydza, soja, tapioka, gryka Wszystkie tłuszcze Cukier, miód Przyprawy, sól, pieprz Kawa, herbata, kakao Pieczywo, ciasta i desery muszą być przygotowywane z produktów niezawierających glutenu Wszystkie produkty oznaczone symbolem „przekreślony kłos” |
Przetwory z pszenicy, żyta, jęczmienia i owsa* Bułki, chleb zwykły, chleb razowy Pieczywo chrupkie Orkisz Kuskus Zwykłe makarony Kasza manna, kasza jęczmienna, owsiana* Pęczak, płatki owsiane* Ciasta, herbatniki, słodycze zawierające gluten Pasztety, parówki itp. o nieznanym składzie |
* W niektórych krajach spożywanie owsa jest dopuszczone (warunkiem jest zapewnienie braku zanieczyszczenia nawet minimalnymi ilościami glutenu pochodzącego z pszenicy, żyta lub jęczmienia)
Analiza przypadku klinicznego
Chłopiec w wieku 22 miesięcy przyjęty został do Kliniki z powodu wymiotów poposiłkowych i biegunki ze śluzem, trwających od ok. 4 miesięcy i wiązanych z zapaleniem oskrzeli leczonym amoksycyliną z kwasem klawulanowym.
Od roku rodzice obserwowali wzdęcia i zachowanie dziecka sugerujące bóle brzucha. Ze względu na brak od 4. m.ż. do chwili hospitalizacji pomiarów masy ciała nikt nie zaobserwował niedoborów. W chwili przyjęcia stwierdzono masę 9420 g (< 3 pc; w pierwszych miesiącach życia masa na 50 pc), wzrost 85,6 cm (10–25 pc); BMI 12,75 (< 3pc według WHO); wsk. Cole’a 81% (dostępna krzywa masy ciała; patrz ryc. 1).
W badaniu przedmiotowym cechy wyniszczenia, bardzo skąpa tkanka podskórna, zanik mięśni pośladków, wzdęcie brzucha, sterczące żebra, różaniec krzywiczy (patrz ryc. 2, 3). Dziecko smutne i apatyczne.
Ryc. 1. Efekty diety bezglutenowej

Ryc. 2–3. Cechy wyniszczenia – skąpa tkanka podskórna, zanik mięśni pośladków, wzdęcia brzucha, sterczące żebra


W badaniach pomocniczych: ↑ INR (1,5); ↓ Hb (9 g%); ↓ MCV(65 fl), ↑ mocznik (50 mg%). Z uwagi na wywiad oraz wygląd dziecka sugerujący celiakię zlecono anty-tTG w klasie IgA i IgG oraz wykonano gastroskopię – już badanie makroskopowe wykazało, że błona śluzowa w części zstępującej dwunastnicy jest pozbawiona struktury kosmkowej, wygładzona, muszelkowana – obraz z dużym prawdodopodobieństwem sugerował celiakię, co znalazło pełne potwierdzenie w uzyskanych wynikach (znacznie podwyższone miano anty-tTG w klasie IgA i IgG oraz zanik błony śluzowej dwunastnicy oceniony przez histopatologa na Marsh 3c).
Rozpoznano celiakię. Zastosowano parenteralnie witaminę K, uzyskując szybką normalizację INR, podano żelazo w dawce terapeutycznej doustnie (5 mg/kg/dobę) wraz z witaminą B6 i kwasem foliowym, także uzyskując powolną poprawę morfologii krwi oraz włączono dietę bezglutenową, obserwując zarówno stosunkowo szybką poprawę masy ciała, jak i normalizację zachowania się dziecka i poprawę jego nastroju. Podwyższone stężenie mocznika będące wynikiem łagodnej przednerkowej niewydolności nerek oraz katabolizmu tkankowego uległo normalizacji po kilku dniach terapii.
Komentarz do przypadku
Jest to przypadek rzadko już spotykanej, klasycznej celiakii, czyli celiakii kwitnącej. Należy sądzić, że właśnie z uwagi na rzadkość występowania nie nasunął lekarzom badającym kilkakrotnie dziecko żadnych skojarzeń i nie wzbudził niepokoju. Można przyjąć, że dziecko nie było oglądane całkowicie rozebrane, badano mu tylko to, co wzbudzało doraźny niepokój, czyli objawy związane z zapaleniem oskrzeli (skądinąd najprawdopodobniej zupełnie niepotrzebnie leczonego antybiotykiem zamiast objawowo sterydami wziewnymi i betamimetykami). Zwraca także uwagę brak wpisów dotyczących masy ciała dziecka oraz niekorzystanie przez lekarzy z siatek centylowych (warto podkreślić, że dziecko miało wykonane wszystkie szczepienia obowiązkowe, więc była możliwość wykonania pomiarów masy ciała i naniesienia ich na siatki centylowe). Wykreślenie krzywej masy ciała na siatkach centylowych zapewne znacznie wcześniej zwróciłoby uwagę na zaburzenia przyrostów masy ciała chorego, a nawet zapewne spadek masy ciała, który musiał mieć miejsce. Na siatce centylowej (ryc. 1) widoczny jest znakomity efekt zastosowanej diety bezglutenowej, choć na pierwsze przyrosty masy czekać trzeba zwykle ok. 4–6 tygodni. Niedokrwistość z niedoboru żelaza jest klasycznym objawem celiakii, gdyż żelazo wchłania się jedynie w dwunastnicy, odcinku najbardziej uszkodzonym w przebiegu celiakii. Wydłużony czas protrombinowy w celiakii klasycznej nie jest zjawiskiem częstym, ale w czasach, gdy takich kwitnących celiakii było w oddziałach znacznie więcej, nie był zjawiskiem niezwykle rzadkim.
PIŚMIENNICTWO
- Husby S., Koletzko S., Korponay-Szabó I.R. European Society for Pediatric Gastroenterology, Hepatology, and Nutritition Guidelines for the diagnostic of coeliac disease. J Pediatr Gastroenterol Nutr. 2012;54:136–160.
- Szajewska H. Postępy w żywieniu i gastroenterologii w 2011 roku. Medycyna Praktyczna Pediatria 2012;1:12–18.
- Mustalahti K., Catassi C., Reunanen A., et al. Coeliac EU Cluster, Project Epidemiology: The prevalence of celiac disease in Europe: Results of a centralized, international mass screening project. Ann. Med. 2010;42: 587–595.
- Green P.H., Jabri B. Coeliac disease. Lancet 2003;362:383–391.
- Shan L., Molberg O., Parrot I., et al. Structural basis for gluten intolerance in celiac sprue. Science 2002;297:2275–2279.
- Tjon J.M., van Bergen J., Koning F. Celiac disease: how complicated can it get? Immunogenetics 2010;62:641–651.
- Hill I.D. What are the sensitivity and specificity of serologic tests for celiac disease? Do sensitivity and specificity vary in different populations? Gastroenterology. 2005; 128 (4 suppl 1): S25–S32.
- Lewis N.R., Scott B.B. Systematic review: the use of serology to exclude or diagnose coeliac disease (a comparison of the endomysial and tissue transglutaminase antibody tests). Aliment Pharmacol Ther. 2006;24:47–54.
- Cataldo F., Marino V., Ventura A., Bottaro G., Corazza G.R. Prevalence and clinical features if selective immunoglobulin A deficiency in coeliac disease: an Italian multicentre study. Italian Society of Paediatric Gastroenterology and Hepatology (SIGEP) and “Club del Tenue” Working Groups on Coeliac Disease. Gut. 1998;42:362–365.